Die Brennstoffzelle
Eine Brennstoffzelle wandelt chemische Energie ohne Umwege über mechanische Energie direkt in elektrische Energie und Wärme um. Diese direkte Umwandlung macht die Brennstoffzelle effizienter als konventionelle und andere Energieumwandlungsformen.
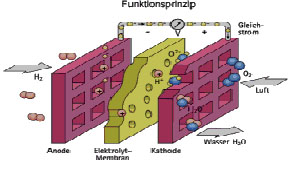
Funktionsprinzip
(anhand einer Polymer-Membran-Brennstoffzelle)
Aufbau (PEM: Proton Exchange Membrane):
- Elektroden (Anode und Kathode)
- Elektrolyte (z. B. PEM)
An der Anodenseite werden Wasserstoffmoleküle (H2) zugeführt, und an der Kathodenseite dagegen führt man Sauerstoffmoleküle zu.
Anodenseite (2 H2 --> 4 H+ +4 e-)
Mit Hilfe von fein verteilten Platin beschichteten Katalysatoren wird das Wasserstoffmolekül zunächst in seine atomaren Bestandteile gespalten. Diese Wasserstoffatome geben je ein negativ geladenes Teilchen ab (Elektronen: e-), die Elektronen fließen über den Verbraucherkreis und leisten dort elektrische Arbeit.
Elektrolyte
Während die Elektronen (e-) elektrische Arbeit über den Verbraucherkreis leisten, wandern die Protonen (H+) durch die Elektrolyte in Richtung Kathodenseite. Die Elektrolyte haben die Eigenschaft, einerseits Ionen zu leiten, andererseits Elektronen (e-) abzustoßen.
Kathodenseite (O2 + 4 e- --> 2 O2-)
Hier werden ebenfalls die zugeführten Sauerstoffmoleküle (O2) katalytisch in ihre atomaren Bestandteile gespalten. Je ein Sauerstoffatom (O) nimmt dann zwei Elektronen auf und wird somit negativ ionisiert (O2-) und geht schließlich mit zwei Protonen(H+) eine Bindung ein. Das Ergebnis ist Wasser (H2O). Bruttoreaktion: 2 H + O2 --> 2 H2O
Vorteile
- hohe Effizienz; Einsparen fossiler Energieträger
- wartungsarm
- kompakt
- niedrige Belastung durch Abgase (außer bei Brenngasgewinnung); keine Stickoxide
- keine Lärmbelästigung
- austauschbare Komponenten durch modulare Bauweise
- gutes Anfahrverhalten / schnelle Reaktion auf Lastwechsel
- Erzeugung von elektrischem Strom bei dezentralen BZ

Kontakt
Exalenca Enertronik
Dipl.-Ing. Abdou Ouedraogo
Wilhelm-Hauff-Str. 12
26721 Emden
Telefon 04921-929840
Mobil 0175-8254907
E-Mail info @ exalenca.de
